Хром
Хром
Хром (лат. Cromium), Cr, химический элемент VI группы периодической системы Менделеева, атомный номер 24, атомная масса 51,996; металл голубовато-стального цвета.
Природные стабильные изотопы: 50 Cr (4,31%), 52 Cr (87,76%), 53 Cr (9,55%) и 54 Cr (2,38%). Из шести искусственных радиоактивных изотопов наиболее важен 51 Cr (период полураспада T1 /2 = 27,8 сут ), который применяется как изотопный индикатор .
Историческая справка. Х. открыт в 1797 Л. Н. Вокленом в минерале крокоите — природном хромате свинца PbCrO4 . Название Х. получил от греческого слова chroma — цвет, краска (из-за разнообразия окраски своих соединений). Независимо от Воклена Х. был открыт в крокоите в 1798 немецким учёным М. Г. Клапротом.
Распространение в природе. Среднее содержание Х. в земной коре (кларк) 8,3?10-3 %. Этот элемент, вероятно, более характерен для мантии Земли , т.к. ультраосновные породы, которые, как полагают, ближе всего по составу к мантии Земли, обогащены Х. (2?10-1 %). Х. образует массивные и вкрапленные руды в ультраосновных горных породах; с ними связано образование крупнейших месторождений Х. (см. Хромовые руды ). В основных породах содержание Х. достигает лишь 2?10-2 %, в кислых — 2,5?10-3 %, в осадочных породах (песчаниках) — 3,5?10-3 %, глинистых сланцах — 9?10-3 %. Х. — сравнительно слабый водный мигрант; содержание Х. в морской воде 0,00005 мг/л.
В целом Х. — металл глубинных зон Земли; каменные метеориты (аналоги мантии) тоже обогащены Х. (2,7?10-1 %). Известно свыше 20 минералов Х. Промышленное значение имеют только хромшпинелиды (до 54% Cr); кроме того, Х. содержится в ряде др. минералов, которые нередко сопровождают хромовые руды, но сами не представляют практической ценности (уваровит , волконскоит, кемерит, фуксит).
А. И. Перельман.
Физические и химические свойства. Х. — твёрдый, тяжёлый, тугоплавкий металл. Чистый Х. пластичен. Кристаллизуется в объёмноцентрированной решётке, а
= 2 885
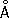 (20 °С); при ~ 1830 °С возможно превращение в модификацию с гранецентрированной решёткой, а
= 3,69
(20 °С); при ~ 1830 °С возможно превращение в модификацию с гранецентрированной решёткой, а
= 3,69
 .
.
Атомный радиус 1,27
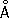 ; ионные радиусы Cr2+
0,83
; ионные радиусы Cr2+
0,83
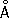 , Cr3+
0,64
, Cr3+
0,64
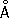 , Cr6+
0,52
, Cr6+
0,52
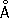 Плотность 7,19 г/см3
; tпл
1890 °С; tкип
2480 °С. Удельная теплоёмкость 0,461 кдж/
(кг
?К.
)
[0,11 кал/(г
?°С)] (25°С); термический коэффициент линейного расширения 8,24?10-6
(при 20 °С); коэффициент теплопроводности 67 вм/
(м
?К
)
[0,16 кал/
(см
?сек
?°С
)]
(20 °С); удельное электросопротивление 0,414 мком
?м
(20°С); термический коэффициент электросопротивления в интервале 20—600 °С составляет 3,01?10-3
. Х. антиферромагнитен, удельная магнитная восприимчивость 3,6?10-6
. Твёрдость высокочистого Х. по Бринеллю 7—9 Мн/м2
(70—90 кгс/см2
).
Плотность 7,19 г/см3
; tпл
1890 °С; tкип
2480 °С. Удельная теплоёмкость 0,461 кдж/
(кг
?К.
)
[0,11 кал/(г
?°С)] (25°С); термический коэффициент линейного расширения 8,24?10-6
(при 20 °С); коэффициент теплопроводности 67 вм/
(м
?К
)
[0,16 кал/
(см
?сек
?°С
)]
(20 °С); удельное электросопротивление 0,414 мком
?м
(20°С); термический коэффициент электросопротивления в интервале 20—600 °С составляет 3,01?10-3
. Х. антиферромагнитен, удельная магнитная восприимчивость 3,6?10-6
. Твёрдость высокочистого Х. по Бринеллю 7—9 Мн/м2
(70—90 кгс/см2
).
Внешняя электронная конфигурация атома Х. 3d5 4s1 . В соединениях обычно проявляет степени окисления +2, +3, +6, среди них наиболее устойчивы Cr3+ ; известны отдельные соединения, в которых Х. имеет степени окисления +1, +4, +5. Х. химически малоактивен. При обычных условиях устойчив к кислороду и влаге, но соединяется с фтором, образуя CrF3 . Выше 600 °С взаимодействует с парами воды, давая Cr2 O3 ; азотом — Cr2 N, CrN; углеродом — Cr23 C6 , Cr7 C3 , Cr3 C2 ; серой — Cr2 S3 . При сплавлении с бором образует борид CrB, с кремнием — силициды Cr3 Si, Cr2 Si3 , CrSi2 . Со многими металлами Х. даёт сплавы (см. Хромовые сплавы ). Взаимодействие с кислородом протекает сначала довольно активно, затем резко замедляется благодаря образованию на поверхности металла окисной плёнки. При 1200 °С плёнка разрушается и окисление снова идёт быстро. Х. загорается в кислороде при 2000 °С с образованием темно-зелёной окиси Х. Cr2 O3 . Помимо окиси, известны др. соединения с кислородом, например CrO, CrO3 , получаемые косвенным путём (подробнее см. Хрома окислы ). Х. легко реагирует с разбавленными растворами соляной и серной кислот с образованием хлорида и сульфата Х. и выделением водорода; царская водка и азотная кислота пассивируют Х.
С увеличением степени окисления возрастают кислотные и окислительные свойства Х. Производные Cr2+ — очень сильные восстановители. Ион Cr2+ образуется на первой стадии растворения Х. в кислотах или при восстановлении Cr3+ в кислом растворе цинком. Гидрат закиси Cr (OH)2 при обезвоживании переходит в CrO4 2- . Соединения Cr3+ устойчивы на воздухе. Могут быть и восстановителями и окислителями. Cr3+ можно восстановить в кислом растворе цинком до Cr2+ или окислить в щелочном растворе до CrO4 2- бромом и др. окислителями. Гидроокись Cr (OH)3 (вернее Cr2 O3 ?nH2 O — амфотерное соединение, образующее соли с катионом Cr3+ или соли хромистой кислоты HCrO2 — хромиты (например, KCrO2 , NaCrO2 ). Соединения Cr6+ : хромовый ангидрид CrO3 , хромовые кислоты и их соли, среди которых наиболее важны хромоты и дихроматы (см. также Хромпик ) — сильные окислители. Х. образует большое число солей с кислородсодержащими кислотами. Известны комплексные соединения Х.; особенно многочисленны комплексные соединения Cr3+ , в которых Х. имеет координационное число 6. Существует значительное число перекисных соединений Х.
Получение. В зависимости от цели использования получают Х. различной степени чистоты. Сырьём обычно служат хромшпинелиды, которые подвергают обогащению, а затем сплавляют с поташом (или содой) в присутствии кислорода воздуха. Применительно к основному компоненту руд, содержащему Cr3+ , реакция следующая:
2FeCr2 O4 + 4К2 СО3 + 3,5O2 = 4K2 CrO4 + Fe2 O3 + 4CO2 .
Образующийся хромат калия K2 CrO4 выщелачивают горячей водой и действием H2 SO4 превращают его в дихромат K2 Cr2 O4 . Далее действием концентрированного раствора H2 SO4 на K2 Cr2 O7 получают хромовый ангидрид CrO3 или нагреванием K2 Cr2 O7 с серой — окись Х. Cr2 O3 .
Наиболее чистый Х. в промышленных условиях получают либо электролизом концентрированных водных растворов CrO3 или Cr2 O3 , содержащих H2 SO4 , либо электролизом сульфата Х. Cr2 (SO4 )3 . При этом Х. выделяется на катоде из алюминия или нержавеющей стали. Полная очистка от примесей достигается обработкой Х. особо чистым водородом при высокой температуре (1500—1700 °С).
Возможно также получение чистого Х. электролизом расплавов CrF3 или CrCl3 в смеси с фторидами натрия, калия, кальция при температуре около 900 °С в атмосфере аргона.
В небольших количествах Х. получают восстановлением Cr2 O3 алюминием или кремнием. При алюминотермическом способе предварительно подогретую шихту из Cr2 O3 и порошка или стружек Al с добавками окислителя загружают в тигель, где реакцию возбуждают поджиганием смеси Na2 O2 и Al до тех пор, пока тигель заполнится Х. и шлаком. Силикотермически Х. выплавляют в дуговых печах. Чистота получаемого Х. определяется содержанием примесей в Cr3 O3 и в Al или Si, используемых для восстановления.
В промышленности в больших масштабах производятся сплавы Х. — феррохром и силикохром .
Применение. Использование Х. основано на его жаропрочности, твёрдости и устойчивости против коррозии. Больше всего Х. применяют для выплавки хромистых сталей (см. Хромаль , Хромель , Хромансиль ). Алюмино- и силикотермический Х. используют для выплавки нихрома , нимоника , других никелевых сплавов и стеллита .
Значительное количество Х. идёт на декоративные коррозионно-стойкие покрытия (см. Хромирование ). Широкое применение получил порошковый Х. в производстве металлокерамических изделий и материалов для сварочных электродов. Х. в виде иона Cr3+ — примесь в рубине , который используется как драгоценный камень и лазерный материал . Соединениями Х. протравливают ткани при крашении. Некоторые соли Х. используются как составная часть дубильных растворов в кожевенной промышленности; PbCrO4 , ZnCrO4 , SrCrO4 — как художественные краски. Из смеси хромита и магнезита изготовляют хромомагнезитовые огнеупорные изделия .
Соединения Х. (особенно производные C6+ ) токсичны.
А. Б. Сучков.
Х. в организме. Х. — один из биогенных элементов , постоянно входит в состав тканей растений и животных. Среднее содержание Х. в растениях — 0,0005% (92—95% Х. накапливается в корнях), у животных — от десятитысячных до десятимиллионных долей процента. В планктонных организмах коэффициент накопления Х. огромен — 10 000 — 26 000. Высшие растения не переносят концентрации Х. выше 3?10-4 моль/л. В листьях он присутствует в виде низкомолекулярного комплекса, не связанного с субклеточными структурами. Необходимость Х. для растений не доказана. У животных Х. участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов (структурный компонент глюкозоустойчивого фактора). Основной источник поступления Х. в организм животных и человека — пища. Снижение содержания Х. в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови и снижению чувствительности периферийных тканей к инсулину.
М. Я. Школьник.
Отравлениях, и его соединениями встречаются при их производстве; в машиностроении (гальванические покрытия); металлургии (легирующие добавки, сплавы, огнеупоры); при изготовлении кож, красок и т.д. Токсичность соединений Х. зависит от их химической структуры: дихроматы токсичнее хроматов, соединения Cr (VI) токсичнее соединений Cr (II), Cr (lll). Начальные формы заболевания проявляются ощущением сухости и болью в носу, першением в горле, затруднением дыхания, кашлем и т.д.; они могут проходить при прекращении контакта с Х. При длительном контакте с соединениями Х. развиваются признаки хронического отравления: головная боль, слабость, диспепсия, потеря в весе и др. Нарушаются функции желудка, печени и поджелудочной железы. Возможны бронхит, бронхиальная астма, диффузный пневмосклероз. При воздействии Х. на кожу могут развиться дерматит, экзема. По некоторым данным, соединения Х., преимущественно Cr (lll), обладают канцерогенным действием. Профилактика отравлений: периодические медицинские осмотры с участием отоларинголога; при гальванических процессах — местная вентиляция в виде бортовых отсосов у ванн, использование перчаток, защитных мазей; при наличии пыли, содержащей Х., применяют респираторы, общие средства пылеподавления и пылеулавливания.
А. А. Каспаров.
Лит.: Салли А. Г., Брэндз Э. А., Хром, 2 изд., М., 1971; Некрасов Б. В., Основы общей химии, М., 1973; Ахметов Н. С., Неорганическая химия, 2 изд., М., 1975; Реми Г., Курс неорганической химии, пер. с нем., т. 1—2, М., 1972—74; Коттон Ф., Уилкинсон Дж., Современная неорганическая химия, пер. с англ., ч. 3, М., 1969; Грушко Я. М., Соединения хрома и профилактика отравлений ими, М., 1964; Bowen Н. J. М., Trace elements in biochemistry, L. — N. Y., 1966.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Что такое хром?
Что такое хром? Хром — это металл. Он твердый и ломкий и очень устойчив к коррозии. Он серебристо-белый, а после полировки приобретает блеск. Он плохо проводит электричество и тепло. Хром нельзя обнаружить в природе в виде металла. Он содержится в нескольких минералах,
Что такое хром?
Что такое хром? Хром — это твердый, ломкий металл серебристо-белого цвета, который практически не поддается коррозии и обладает низкой элект-ро- и теплопроводностью.В чистом виде хром в природе никогда не встречается. Он входит в состав ряда минералов, в основном