11.1. Острый пиелонефрит
11.1. Острый пиелонефрит
Пиелонефрит – неспецифическое инфекционно-воспалительное заболевание почек с одновременным или последовательным поражением чашечно-лоханочной системы почек и тубулоинтерстициальной ткани.
Патофизиология
Острый пиелонефрит (ОП) – инфекция, которая может быть причиной образования абсцессов, потери органа, развития почечной недостаточности, уросепсиса и септического шока с полиорганной недостаточностью, гибели пациента. Инфекции мочевых путей составляют не менее 40% всех госпитальных инфекций, основной причиной которых является катетеризация мочевого пузыря.
К обструктивным/структурным изменениям мочевыделительной системы, предрасполагающим к развитию осложненного ОП, относят: почечнокаменную болезнь, заболевание простаты и парауретральных желез (доброкачественная гиперплазия и рак простаты, простатит, везикулит), нарушение строения и стриктуры мочеточников, уретры, дивертикулы мочевого пузыря, почечные кисты, фистулы, анатомические аномалии мочевых путей и др. Функциональные нарушения мочевыделительной системы составляют нейрогенный мочевой пузырь, рефлюксы (обратный ток мочи) на разных уровнях. Риск ОП возрастает при наличии сопутствующих заболеваний, таких, как сахарный диабет (СД), инфекция мочевого тракта у детей, трансплантация почки, иммуносупрессия, злоупотребление анальгетиками, наличие инородных тел (постоянный стент, нефростома), а также при беременности.
Различают неосложненный и осложненный острый пиелонефрит; по распространенности – односторонний и двусторонний.
При неосложненном ОП инфекционно-воспалительный процесс возникает в интактных почках преимущественно у молодых женщин с отсутствием предшествующих мочевых или вагинальных инфекций, анатомических или функциональных нарушений мочевого тракта. Развитие осложненного ОП связано с нарушением пассажа мочи из верхних мочевыводящих путей, обусловленным структурными изменениями, обструктивными заболеваниями урогенитального тракта.
Наиболее частыми возбудителями неосложненного ОП являются энтеробактерии, среди которых в 90% случаев выявляется кишечная палочка, реже протей, клебсиелла – около 10%. У молодых сексуально активных женщин в роли возбудителя часто выступает стафилококк. При осложненном ОП увеличивается спектр потенциальных возбудителей заболевания, возрастает значение протея, синегнойной палочки, увеличивается доля золотистого стафилококка, энтерококков и грибов.
Основным наиболее распространенным путем инфицирования мочевых путей и почек является уриногенный (восходящий). При этом микроорганизмы попадают в почку из нижних отделов мочевыводящих путей, заселенных обитающей в кишечнике уропатогенной флорой. В результате ретроградного тока мочи и продвижения микроорганизмов по слизистой мочевых путей, а также повышения внутрипочечного давления, лежащего в основе различных рефлюксов, обеспечивается дальнейшее обсеменение микроорганизмами ткани почки и возникновение воспалительного процесса. Гораздо реже встречается гематогенный путь распространения инфекции. Вторичные очаги инфекции редко являются причиной инфекции почек, однако появление абсцессов в корковом веществе наблюдается только у пациентов с предрасполагающими факторами (СД, иммуносупрессия).
Клиническая картина
Клиническая картина ОП в значительной мере варьирует в зависимости от предшествующего состояния почек и мочевых путей, степени нарушения пассажа мочи, состояния организма, возраста, пола, сопутствующих заболеваний и характеризуется развитием токсико-интоксикационного синдрома и локальных признаков инфекционного процесса.
При неосложненном ОП преобладают общеклинические системные признаки инфекционного процесса, в то время как местные признаки заболевания выражены слабо или отсутствуют. Как правило, в этих случаях наблюдаются картина общего инфекционного заболевания или сепсиса без видимых признаков поражения почек либо симптомы «острого живота», менингита, паратифа и др.
Заболевание начинается внезапно, клиническая картина разворачивается в течение суток или нескольких часов. Состояние пациента тяжелое, температура тела повышается до 38 – 40 °С, часто сопровождается потрясающим ознобом, проливным потом. Другими проявлениями болезни могут быть такие признаки выраженной общей интоксикации, как общая слабость, утомляемость, отсутствие аппетита, жажда, артралгии и миалгии, сердцебиение, головная боль, тошнота и рвота, иногда спутанность сознания, артериальная гипотония, картина бактериемического шока.
Проявлением местных симптомов заболевания является односторонняя или двухсторонняя боль низкой или средней интенсивности, тупого или ноющего характера в поясничной области. Иногда пациенты могут испытывать неприятные ощущения в поясничной области, чувство тяжести или, наоборот, интенсивную боль распирающего характера; реже боль возникает в боковых отделах живота.
Для детей характерна выраженность интоксикационного синдрома и развитие так называемого абдоминального синдрома, при котором выраженные боли возникают не в поясничной области, а в животе.
Расстройства мочеиспускания для собственно неосложненного ОП не характерны, но могут иметь место при уретрите и цистите, на фоне которых развился восходящий пиелонефрит. Начало заболевания с симптомов острого цистита характерно преимущественно для женщин: учащенное (поллакиурия – каждые 30 – 60 мин) императивное мочеиспускание с малым количеством мочи при однократном мочеиспускании, рези в конце мочеиспускания, боль в надлобковой области, усиливающаяся при пальпации и наполнении мочевого пузыря. Следует подчеркнуть независимость расстройств мочеиспускания от времени суток, движения или покоя.
При физикальном исследовании помимо симптомов интоксикации выявляют напряжение мышц в поясничной области или передней брюшной стенки, болезненность в реберно-позвоночном углу с одной или обеих сторон при поколачивании и при глубокой пальпации, а также болезненность при пальпации живота в области проекции почек.
При осложненном ОП, обусловленном нарушением оттока мочи из почки, в острой фазе заболевания наблюдается характерная смена симптомов. Как правило, ухудшение состояния пациента совпадает с резким усилением боли высокой интенсивности в поясничной области или с приступообразным характером боли вследствие нарушения оттока мочи из почечной лоханки. На высоте болей возникает озноб, который сменяется жаром и резким повышением температуры тела. Затем температура тела критически падает до субфебрильной, что сопровождается обильным потоотделением. Интенсивность боли в области почки постепенно снижается вплоть до ее исчезновения. Однако если препятствие оттоку мочи не устранено, после нескольких часов улучшения самочувствия, наряду с усилением боли, наступает и новый приступ почечной инфекции.
Между тяжестью инфекционно-воспалительных изменений в почке и общим состоянием пациента не всегда отмечается взаимосвязь. У пациентов с СД, ослабленных, а также при наличии или на фоне иммунодефицитных состояний, клинические проявления почечной инфекции минимальны, отсутствуют или развивается атипичная, стертая клиническая картина. У 30 – 50% пациентов в течение двух месяцев после трансплантации почки на фоне иммуносупрессии и послеоперационного везикоуретрального рефлюкса развивается ОП.
У лиц пожилого и старческого возраста ОП отличается значительным разнообразием клинических симптомов, развивающихся на фоне сопутствующих полиморбидных заболеваний, нарушений функционального состояния органов, в частности хронической почечной и сердечной недостаточности. Кроме классического клинического варианта ОП, у трети пациентов отсутствует лихорадка, заболевание протекает практически бессимптомно или характеризуется интоксикационным синдромом с мозговыми, желудочно-кишечными или легочными симптомами.
Диагноз ОП должен подозреваться при появлении клинических симптомов инфекции после предшествующей антибактериальной терапии или наличии выраженного токсико-инфекционного синдрома при отсутствии местной симптоматики. С возрастом снижается частота односторонних форм ОП, и к концу восьмого десятилетия жизни, особенно у мужчин, односторонние процессы практически не встречаются и нарастают наиболее опасные гнойно-обструктивные формы.
У беременных ОП чаще всего возникает на 22-28-й неделе беременности и оказывает неблагоприятное влияние на течение беременности и состояние плода. Так, отмечается значительная частота гестозов, угрозы прерывания беременности, преждевременных родов, хронической фетоплацентарной недостаточности, хронической гипоксии и внутриутробного инфицирования плода, высокая перинатальная заболеваемость и смертность.
К осложнениям ОП относят: бактериемический (эндотоксический) шок, уросепсис, некроз почечных сосочков, абсцессы в почках, паранефрит, острую почечную недостаточность (ОПН), смерть.
Лабораторная диагностика
При лабораторном исследовании обнаруживают изменения в анализе крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево, токсическую зернистость лейкоцитов, повышение СОЭ. В тяжелых случаях возможно умеренное снижение уровня гемоглобина.
В анализах мочи относительная плотность может быть снижена, монотонна; умеренная протеинурия. В осадке мочи выявляют лейкоцитурию или пиурию, гиалиновые, эпителиальные и лейкоцитарные цилиндры. Почечное происхождение лейкоцитурии подтверждает наличие в моче лейкоцитарных цилиндров. Микрогематурия (реже макрогематурия) может наблюдаться при наличии конкремента, цистита, вследствие некротического паппиллита, повреждения форникального аппарата.
Следует отметить, что при осложненном (обструктивном) ОП и при апостематозном нефрите в связи с локализацией гнойников в корковом веществе почки, в течение нескольких дней изменения в анализах мочи могут отсутствовать.
Этиологическая диагностика
Важным этапом этиологической диагностики ОП является бактериологическое исследование. Необходимым условием достоверности результатов исследования является правильность забора мочи и крови, и что особенно важно – до начала антибактериальной терапии.
Окраска нецентрифугированной мочи по Граму позволяет получить предварительные ориентировочные данные о характере возбудителя. Основой диагностики инфекций мочевыводящих путей является определение бактериурии путем количественного определения бактерий в средней порции мочи, полученной при свободном мочеиспускании. В некоторых случаях (у пациентов с мочевым катетером) достоверные результаты могут быть получены при надлобковой пункции мочевого пузыря.
Диагностическими критериями истинной бактериурии являются значения кишечной палочки и других грамотрицательных микроорганизмов ?105 КОЕ (колоние-образующих единиц) уропатогенов/мл в образце средней порции мочи у женщин с неосложненным ОП или ?104 КОЕ уропатогенов/мл у мужчин и у женщин с осложненным ОП.
Для пиогенных кокков или протея достоверной считается бактериурия при меньшем количестве микробных тел в единице объема мочи – 104-103 КОЕ уропатогенов/мл мочи. В образце, полученном при надлобковой пункции мочевого пузыря, любое количество бактерий является клинически значимым.
Необходимо учитывать, что частота выделения бактерий из мочи снижается при предшествующей исследованию антибактериальной терапии, у пациентов с гнойно-деструктивными заболеваниями (около 30%), при нарушении пассажа мочи из пораженной почки. Наиболее информативным материалом для микробиологического исследования является материал, полученный интраоперационно (при осложненном ОП).
Кулыуральное исследование мочи (посев на питательные среды, выделение чистой культуры возбудителя и определение его чувствительности к препаратам) необходимо проводить во всех случаях, особенно в стационаре.
Визуализирующие методы исследования
Алгоритм экстренных исследований при ОП включает ультразвуковое исследование (УЗИ), рентгенологические и радионуклидные методы. Ультразвуковое сканирование почек с применением цветовой допплерографии является доступным первичным методом верификации и характеристики патологических процессов, позволяет выявить увеличение почки/почек в размерах, ограничение их подвижности при дыхании, гипоэхогенную структуру почечной ткани, утолщение почечной паренхимы.
При осложненном ОП регистрируются асимметричные изменения в почках: пораженная почка увеличена в объеме с неравномерными контурами, паренхима утолщена и уплотнена, чашечно-лоханочные структуры расширены и деформированы, сосочки уплотнены. Кроме того, в ряде случаев диагностируются не только признаки ретенции, но также и ее причины, например тени в лоханках (микролиты, мелкие камни, склероз сосочков), обтурирующие камни, кисты, аномалии развития, опухоли и др.
При апостематозном пиелонефрите ультразвуковая картина такая же, как в фазе серозного воспаления (увеличение почек в размерах, ограничение их подвижности). Для карбункула почки характерно наличие гипоэхогенного участка без четких контуров с набуханием внешнего контура почки. При формировании абсцесса почки определяется гипоэхогенное образование (полость) с четкими контурами (капсула абсцесса), иногда с неоднородными анэхогенными участками в центре (жидкий гной). При выходе гнойного процесса за пределы капсулы почки (развитие паранефрита) определяется нечеткость паранефральной клетчатки с наличием в ней гипо– и анэхогенных компонентов.
На обзорной рентгенограмме может быть выявлено увеличение размеров почки, набухание ее контура (при карбункуле и абсцессе), нечеткость контура большой поясничной мышцы на стороне поражения (отек паранефральной клетчатки, паранефрит), наличие теней конкрементов.
При экскреторной урографии можно установить: асимметрию размеров почек, увеличение в объеме пораженной почки, снижение тонуса верхних мочевых путей, уплощенность и закругленность углов форниксов, сужение и вытянутость чашечек, сближение их, пиелоренальные рефлюксы, пиелоэктазии. В случае спазма сосочковых сфинктеров выявляется интенсивная тень почки, так называемый «симптом белой почки» Подвижность почки при ортопробе ограничена, отсутствует контур поясничной мышцы. При наличии карбункула или абсцесса почки, кроме уменьшения подвижности почки, обнаруживаются неравномерность наружных ее контуров и деформация лоханки, сдавливание чашечек в зоне поражения вплоть до их «ампутации».
Информативной является компьютерная рентгеновская томография, особенно при подозрении на деструктивный ОП, позволяющая составить четкое представление о массе и плотности паренхимы почки, состоянии лоханки, сосудистой ножки, паранефральной клетчатки.
При непереносимости контрастных веществ, у пациентов с высоким риском повреждения почек контрастом, при ОПН или ХПН, когда невозможно контрастирование мочевых путей, методом выбора является магнитно-резонансная урография.
С помощью инфракрасной термографии выявляют повышение температуры над пораженной почкой на 1,4-2° по сравнению со здоровой стороной. Как правило, при серозном воспалении отсутствуют мелкоточечные очаги свечения в области забрюшинного пространства. Усиление гипертермии, в том числе по площади ее распространения, а также появление множества мелких очагов гипертермии в области забрюшинного пространства являются признаками перехода серозного воспаления в гнойное.
Дифференциальная диагностика
В дифференциально-диагностическом отношении нередко возникают проблемы разграничения ОП от таких инфекций, как пневмония, абсцесс легкого, сепсис, бактериальный эндокардит, некоторые кишечные инфекции, в частности сальмонеллез (особенно в случаях его осложнения шоком).
Иногда ОП может симулировать острую хирургическую патологию: аппендицит, холецистит, панкреатит, аднексит; онкологические заболевания: гемобластоз, аденокарцинома почки, лимфогранулематоз. У пожилых пациентов с впервые возникшими симптомами ОП и гематурией исключают злокачественную опухоль мочевых путей, в том числе и почек.
Септикопиемия с образованием метастатических гнойников в других органах (эндокард, менингит, скелетная система, глаза) и присоединение поражения печени нередко маскируют первичный очаг в почке и приводят к смерти пациента до наступления уремии вследствие гнойного менингита, абсцедирующей пневмонии.
Стратегия лечения зависит от тяжести заболевания и преследует три цели: устранение нарушения пассажа мочи, антимикробную терапию и при необходимости патогенетическое лечение.
Антибактериальная терапия
До начала применения антибактериальных препаратов необходимо провести взятие материала для бактериологического исследования мочи (крови по показаниям) с идентификацией возбудителя и определения его чувствительности к антибиотикам, оценить функцию почек.
Лечение неосложненного ОП базируется на незамедлительной адекватной антибактериальной терапии.
Напротив, при осложненном ОП антибактериальные препараты назначают только после восстановления оттока
мочи от пораженной почки.
При обструктивном ОП необходимо установить ретенционное поражение мочевых путей, которое требуется устранить в первую очередь, поскольку суть патологического процесса и нередко его исход (вплоть до потери органа или даже смерти) определяет, как правило, уростаз. Вопрос о методе восстановления оттока мочи зависит от причины нарушения уродинамики и ее последствий, тяжести состояния, пола, возраста, сопутствующих заболеваний и решается индивидуально.
К органосохраняющим операциям относят: катетеризацию мочеточника, установку стента, чрескожную пункционную или операционную нефростомию. При любых вариантах гнойного пиелонефрита выполняется декапсуляция почки, при апостематозном пиелонефрите – вскрытие апоспем, при наличии карбункула почки – рассечение и иссечение карбункула, при абсцессе почки – вскрытие абсцесса и иссечение его стенки.
Антибактериальную терапию проводят эмпирически до результатов бактериологического исследования мочи и корректируют после их получения.
Принципы эмпирической антибактериальной терапии:
– предположение возможного спектра микроорганизмов, являющихся наиболее частыми возбудителями неосложненного или осложненного ОП, позволяет определить их природную чувствительность к антибактериальным препаратам;
– использование данных о чувствительности к антибиотикам флоры, выделенной от пациентов с уроинфекциями, и сведения о локальной резистентности антибиотиков;
– анализ предшествующей неэффективной антибактериальной терапии и спектр ее антимикробного действия;
– назначение антибактериальных препаратов в адекватных дозах, максимально перекрывающих возможный спектр наиболее вероятных возбудителей заболевания;
– антибактериальные препараты должны выводиться почками, создавать высокую концентрацию в моче и оказывать минимальное воздействие на микрофлору кишечника и влагалища;
– недопустимо использование плохо всасывающихся из желудочно-кишечного тракта антибиотиков, ведущих к быстрому развитию дисбактериоза кишечника;
– необходимо учитывать оптимальное соотношение стоимость/эффективность лечения (адекватная антибактериальная терапия всегда более эффективна как в клиническом, так и в экономическом плане по сравнению с дешевыми, но мало– или неэффективными препаратами).
Оптимально проведение ступенчатой терапии – лечение начинается с парентерального введения антибиотика до нормализации температуры тела с последующим переходом на прием внутрь того же препарата. Длительность терапии 10-14 дней, но иногда требует увеличения до 21 суток.
В качестве стартовой эмпирической терапии неосложненного ОП препаратами выбора являются: фторхинолоны (левофлоксацин, пефлоксацин, ципрофлоксацин), второй линии – ингибиторозащищенные пенициллины (амоксициллин/клавуланат), цефалоспорины II и III генерации (цефуроксим, цефотаксим). Аминогликозиды (гентамицин, амикацин, нетилмицин, тобрамицин) являются альтернативными препаратами (табл. 6, 7).
Таблица 6
Эмпирическая антибактериальная терапия

Таблица 7
Дозирование антибактериальных препаратов при остром пиелонефрите
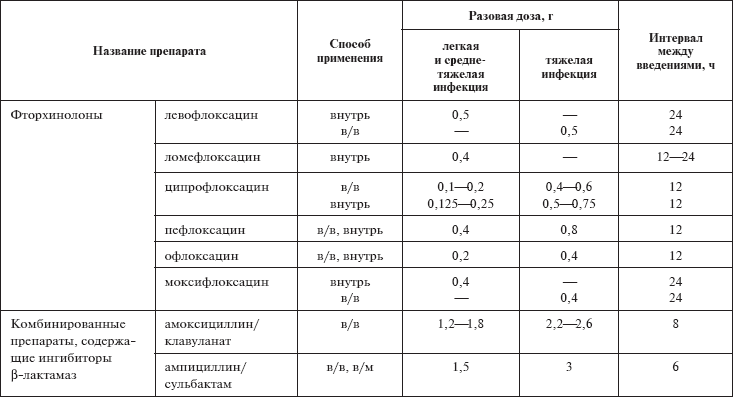
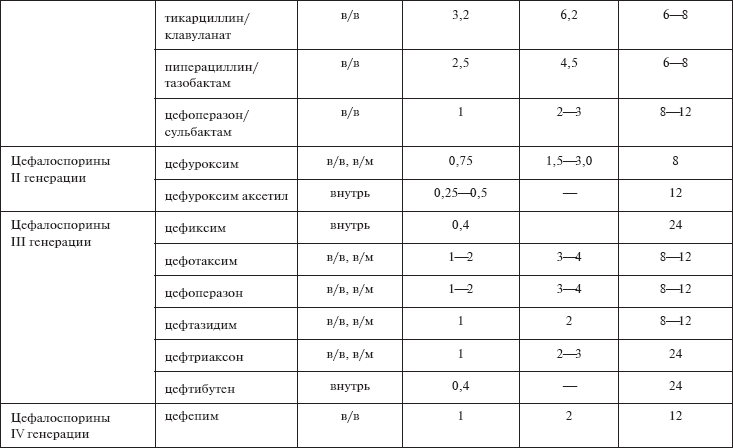

В случае неэффективности стартового режима или тяжелого течения инфекции должны применяться препараты широкого спектра: фторхинолоны (если они не применялись в стартовой терапии), антисинегнойные цефалоспорины III генерации или карбапенемы в виде монотерапии или в комбинации с аминогликозидами.
Основная цель лечения осложненных ИМП – купирование клинических проявлений инфекционно-воспалительного процесса в почках, профилактика уросепсиса и рецидивов. При осложненном ОП препаратами выбора являются ингибиторозащищенные пенициллины (амоксициллин/клавуланат, ампициллин/сульбактам), цефалоспорины II-IV поколения (цефуроксим, цефотаксим, цефепим), ингибиторозащищенные цефалоспорины (цефоперазон/сульбактам), альтернативными препаратами – карбапенемы (имипенем, меропенем, эртапенем), комбинация аминогликозидов и ?-лактамов.
Известно, что одной из характерных нежелательных реакций для аминогликозидов является нефротоксичность. Поэтому аминогликозиды оправдано использовать только у госпитализированных пациентов, при этом необходимо учитывать такие факторы риска, как наличие нарушений функции почек, престарелый возраст, повторное применение препарата с интервалом менее года, одновременное применение других нефротоксичных препаратов (амфотерицин В, полимиксин В, ванкомицин, петлевые диуретики, циклоспорин). Рекомендуется однократное введение полной суточной дозы препарата.
При пиелонефрите беременных препаратами выбора являются ингибиторозащищенные пенициллины (амоксициллин/клавуланат, ампициллин/сульбактам) или цефалоспорины II-IV поколения (цефуроксим, цефотаксим, цефепим), которые также назначают внутривенно с последующим переходом на прием внутрь. Общая длительность антибактериальной терапии не менее 14 дней.
При подозрении на госпитальную инфекцию предпочтение необходимо отдавать цефалоспоринам IV поколения (цефепим), ингибиторозащищенным цефалоспоринам (цефоперазон/сульбактам) или карбапенемам. Карбапенемы рассматриваются как препараты резерва, но при риске потери органа, угрожающих жизни инфекциях могут быть рассмотрены в качестве первоочередной эмпирической терапии. Преимуществом карбапенемов является активность, перекрывающая практически весь спектр вероятных возбудителей пиелонефритов.
При гнойных формах ОП в качестве монотерапии можно использовать только имипенем, а в качестве комбинированной терапии – цефтазидим (цефалоспорин III поколения), обладающий высокой активностью в отношении актуальных грамотрицательных возбудителей, и ванкомицин (препарат группы гликопептидов), активный в отношении грамположительной флоры. Альтернативой цефтазидиму может быть цефепим. Для усиления указанных комбинаций при инфекционном процессе, вызванном клебсиеллами – продуцентами ?-лактамаз расширенного спектра, – необходимо дополнительно назначать аминогликозиды.
При подозрении на метициллинорезистентную стафилококковую инфекцию препаратами выбора являются препараты из группы гликопептидов (ванкомицин) и линезолид.
До полного устранения факторов риска эффективное лечение без рецидивов инфекции обычно не достигается, поэтому посев мочи следует производить через 5-9 сут после завершения лечения и через 4-6 нед спустя.
Антибиотики, не рекомендуемые для эмпирической терапии. В настоящее время аминопенициллины и котримоксазол в силу высокой устойчивости уропатогенов не могут рекомендоваться для терапии ОП. В России популярные средства лечения ИМП – нитроксолин, нитрофурантоин, нефторированные хинолоны (налидиксовая, оксолиновая, пипемидиевая кислоты) в настоящее время потеряли свое лидирующее положение. Эти препараты не создают высоких концентраций в паренхиме почек, обладают более низкой микробиологической активностью по сравнению с фторхинолонами, индуцируют развитие резистентности.
Первая помощь
• Установите мочеточниковый катетер или стент.
• Установите катетер в мочевой пузырь при подозрении на пузырно-мочеточниковый рефлюкс.
• Установите систему для внутривенного введения растворов.
• Измерьте температуру тела.
• Возьмите общий анализ мочи и анализ мочи на чувствительность к антибиотикам.
• Определите уровень азотистых шлаков.
• Возьмите кровь на электролиты (калий, натрий).
Последующие действия
• Постоянно контролируйте жизненно важные параметры пациента.
• Проводите ежедневную термометрию.
• Проведите этиопатогенетическую антибактериальную терапию.
• Подготовьте пациента к нефростомии.
• Постоянно контролируйте показатели анализов мочи и крови, азотистых шлаков.
Превентивные меры
• Необходимо проводить лечение основного заболевания, которое может привести к развитию острого пиелонефрита (мочекаменной болезни и аденомы предстательной железы, а также всех состояний, сопровождающихся нарушением оттока мочи из почки).
• Беременным женщинам, особенно с многоплодием, многоводием, с крупным плодом и с узким тазом, необходимо не реже 1 раза в месяц проводить бактериологический анализ мочи и исследование уродинамики.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава 30 Острый пиелонефрит
Глава 30 Острый пиелонефрит Острый пиелонефрит-острое воспаление почек и почечных лоханок.Для этого заболевания характерна триада симптомов: повышение температуры, боль в поясничной области и расстройства мочеиспускания. Чаще всего заболевание связано с простудой
11.1. Острый пиелонефрит
11.1. Острый пиелонефрит Пиелонефрит – неспецифическое инфекционно-воспалительное заболевание почек с одновременным или последовательным поражением чашечно-лоханочной системы почек и тубулоинтерстициальной ткани.ПатофизиологияОстрый пиелонефрит (ОП) – инфекция,
Пиелонефрит
Пиелонефрит Это воспалительное заболевание почек инфекционной природы. Может поражаться только одна почка – тогда говорят об одностороннем пиелонефрите, либо две почки– тогда процесс двусторонний.Инфекционная причина заболевания чаще всего представлена кишечной
Пиелонефрит
Пиелонефрит Лечение, хотя бы профилактическое, необходимо проводить постоянно. Каждую весну и осень необходимо на протяжении месяца употреблять растительные сборы. Списки сборов, рекомендуемых к использованию, приведены ниже. Для использования сборов необходимо
Пиелонефрит
Пиелонефрит Больные острым пиелонефритом нуждаются в срочной госпитализации и строгом постельном режиме. В диете должно преобладать большое количество легкоусвояемых белков, жиров и углеводов, витаминов и минеральных солей. Обильное питье (клюквенный, брусничный морс,
Пиелонефрит
Пиелонефрит Общие сведенияПиелонефрит – острое или хроническое инфекционно-воспалительное заболевание почек, характеризующееся поражением самой ткани почки и чашечно-лоханочной системы. Возбудители – энтерококк, протей, стафилококки, стрептококки, кишечная палочка
Пиелонефрит
Пиелонефрит Пиелонефрит — острое или хроническое инфекционно-воспалительное заболевание почек, характеризующееся поражением чашечно-лоханочной системы (1) и самой ткани почки (2). Возбудители — энтерококк, протей, стафилококки, стрептококки, кишечная палочка и другие
Пиелонефрит
Пиелонефрит Пиелонефрит – инфекционно-воспалительное заболевание почек, характеризующееся поражением чашечно-лоханочной системы и самой ткани почки.Развитие заболевания в первую очередь зависит от общего состояния и сопротивляемости организма инфекциям
Пиелонефрит
Пиелонефрит Пиелонефрит – микробно-воспалительный процесс в чашечно-лоханочной системе и интерстициальной ткани почек.Этиология. Вызывается грамотрицательной микробной флорой (кишечная палочка, протей, синегнойная палочка), реже грамположительными микроорганизмами
Острый пиелонефрит
Острый пиелонефрит Причины и симптомы Пиелонефрит – это воспалительное заболевание, поражающее почечную лоханку. Очень часто эта болезнь почек встречается у детей, уступая по частоте только заболеваниям дыхательной системы.Причинами возникновения пиелонефрита могут
Хронический пиелонефрит
Хронический пиелонефрит Хронический пиелонефрит – хроническое инфекционно-воспалительное заболевание почек с преимущественным поражением канальцев, чашечек, лоханок и интерстициальной ткани почек.ЭтиологияЗаболевание вызывают различные микроорганизмы и их
Пиелонефрит
Пиелонефрит Пиелонефрит – инфекционно-воспалительное заболевание почек с поражением канальцев, чашечек, лоханок и интерстициальной ткани почек.ЭтиологияПатологию вызывают различные микроорганизмы и их ассоциации. Чаще возбудителем является кишечная палочка.Пути
Пиелонефрит
Пиелонефрит Пиелонефрит — инфекционно-воспалительное заболевание почек с поражением канальцев, чашечек, лоханок и интерстициальной ткани почек.ЭтиологияПатологию вызывают различные микроорганизмы и их ассоциации. Чаще возбудителем является кишечная палочка.Пути
Пиелонефрит
Пиелонефрит Пиелонефрит – бактериально-воспалительное заболевание почек с преимущественным поражением канальцев, чашечно-лоханочной системы, интерстиция. Одно из самых распространенных заболеваний мочевыделительной системы у детей. Девочки болеют значительно чаще,